Парвовирус B19
Содержание:
Особенности репликации
Поглощенный парвовирус поставляет геном в ядро клетки, где однонитевая ДНК преобразуется в двунитевую ДНК клеточными факторами и ДНК-полимеразой. Двунитевая ДНК-версия вирусного генома требуется для транскрипции и репликации. Репликация происходит только в растущих клетках. Вирусные белки синтезируются в цитоплазме и затем возвращаются в ядро, где собираются вирионы. В результате ядро и цитоплазма клетки дегенерируют. Вирусы освобождаются в результате лизиса клетки.
По способности к размножению в клетках хозяина парвовирусы делят на две группы — дефектные (род Dependovirus) и автономные (остальные вирусы семейства Parvoviridae). Автономные парвовирусы способны к самостоятельной репродукции, и для этого они используют соответствующие ферменты клетки хозяина, прежде всего клеточную ДНК-полимеразу.
Репликация автономных парвовирусов происходит в ядрах клеток, находящихся в S-фазе клеточного цикла, то есть во время удвоения клеточной ДНК. Репликация парвовирусов, как правило, ограничена активно пролиферирующими тканями, что может вызывать аномалии развития у эмбрионов и поражения тканей новорожденного. Во взрослом организме парвовирусная инфекция часто протекает бессимптомно. Многие парвовирусы способны активно реплицироваться в трансформированных и/или раковых клетках, не затрагивая при
этом нормальные клетки организма. Именно это их свойство позволяет рассматривать парвовирусы как простейшие ДНК-содержащие вирусы, обладающие выраженной онколитической активностью.
Как и почему развивается заболевание
Парвовирусная инфекция у детей и у взрослых обычно развивается вне зависимости от сезона. Исключением является эритема парвовирусного происхождения – ее вспышки наблюдаются в основном зимой и весной. Вне стен школ, детских садов, прочих коллективных учреждений случаи заболевания единичны, заразиться вирусом могут люди, ухаживающие за больным ребенком, члены семьи. Смертность при формировании патологии очень низкая.
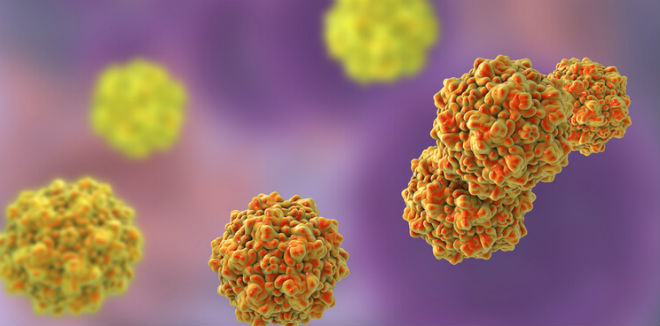 Возбудитель инфекции В19 представляет собой небольших размеров болезнетворный микроорганизм, у которого отсутствует внешняя оболочка. И при этом вирус неплохо сопротивляется внешнему воздействию. Даже при замораживании и нагревании до температуры 600С он не останавливает свое развитие. Не менее стойко микроорганизм сопротивляется липидным растворителям и дезинфицирующим средствам.
Возбудитель инфекции В19 представляет собой небольших размеров болезнетворный микроорганизм, у которого отсутствует внешняя оболочка. И при этом вирус неплохо сопротивляется внешнему воздействию. Даже при замораживании и нагревании до температуры 600С он не останавливает свое развитие. Не менее стойко микроорганизм сопротивляется липидным растворителям и дезинфицирующим средствам.
Пик патологического воздействия приходится на период виремии – активно циркулируя с током крови В19 обнаруживается и в мокротах, и в отделяемом из глотки. Рассматриваемая инфекционная болезнь распространяется пятью способами:
| Наименование способа распространения | Особенности передачи инфекции |
|---|---|
|
Воздушно-капельный |
Самый быстрый и часто встречающийся способ |
|
Трансплантационный |
В процессе пересадки органов, если донором является носитель |
|
Гемотрансфузионный |
В случае переливания зараженной донорской крови либо ее составляющих |
|
Вертикальный |
Беременная женщина, зараженная вирусом, передает заболевание плоду |
|
Контактный |
При общении инфекция передается крайне редко |
Существует две фазы развития парвовирусной патологии у ребенка и взрослого пострадавшего:
- Виремия. На этой стадии вирус проникает во все участки организма вместе с циркулирующей кровью. Период длится на протяжении 5-7 суток, симптомы при этом включают жар и общую слабость, чувство разбитости, мышечные и суставные боли, зуд. В течение этого времени микробы активно выделяются организмом носителя, заражая окружающих. Через несколько дней от начала заражения в крови наблюдается уменьшение количества тромбоцитов и лимфоцитов, снижается уровень гемоглобина.
- На втором этапе наблюдается остановка виремии и образование IgM, еще через несколько суток начинается выработка антител IgG. Они могут наблюдаться в крови в течение неопределенного временного промежутка. В это время симптомы представляют собой кожные высыпания, формируется артрит и артралгия.
 В целом инкубационный период длится в течение от 4 суток до двух недель, в некоторых случаях затягиваясь до 21 дня. В периоды эпидемий из всех случаев на долю школьников приходится от 20 до 60%. Специалисты выделяют два вида патологии:
В целом инкубационный период длится в течение от 4 суток до двух недель, в некоторых случаях затягиваясь до 21 дня. В периоды эпидемий из всех случаев на долю школьников приходится от 20 до 60%. Специалисты выделяют два вида патологии:
- Врожденная, обычно проявляющаяся водянкой плода либо врожденной анемией хронического характера.
- Приобретенная, которую в соответствии со степенью тяжести разделяют на протекающую в легкой форме, средней либо тяжелой. По типу заболевание может быть типичным либо атипичным.
В соответствии с длительностью течения патологии определяют острую, затяжную и хроническую форму. Первая протекает на протяжении до месяца, вторая – не больше трех месяцев, третья – свыше 90 суток.
Примечания код
- Атлас по медицинской микробиологии, вирусологии и иммунологии : Учебное пособие для студентов медицинских вузов / Под ред. А. А. Воробьева, А. С. Быкова. — М. : Медицинское информационное агентство, 2003. — С. 114. — ISBN 5-89481-136-8.
- Maxwell I. H., Terrell K. L., Maxwell F. (2002). Autonomous parvovirus vectors. Methods 28(2): 168—181.
- Tattersall P. (2006). The evolution of parvoviral taxonomy. In the parvoviruses. ed. J. R. Kerr, M. E. Bloom, R. M. Linden et al. Hodder Arnold: London P. 5—14.
- Berns K. I. (1990). Parvovirus replication. Microbiol Rev. 54(3): 316—329.
- Rommelaere J., Giese N., Cziepluch C., Cornelis J. J. Parvoviruses as anti-cancer agents. (2005). In Viral therapy of human cancers. ed. J.G. Sinkovics, J.C. Horvath. Marcel Dekker: New York Р. 627—675.
- Rommelaere J., Cornelis J.J. (1991). Antineoplastic activity of parvoviruses. J Virol Methods 33(3): 233—251.
- ↑ Cornelis J. J., Deleu L., Koch U. et al. (2006). Parvovirus oncosuppression in The parvoviruses. Hodder Arnold: London Р. 365—384.
- Randall R. E., Goodbourn S. (2008). Interferons and viruses: an interplay between induction, signalling, antiviral responses and virus countermeasures. J Gen Virol. 89(1): 1—47.
- Rommelaere J., Geletneky K., Angelova A.L. et al. (2010). Oncolytic parvoviruses as cancer therapeutics. Cytokine Growth Factor Rev. 21(2—3): 185—195.
- Cotmore S.F., Tattersall P. (1987). The autonomously replicating parvoviruses of vertebrates. Adv Virus Res. 33: 91—174.
- Niskanen E. A., Ihalainen T. O., Kalliolinna O. et al. (2010). Effect of ATP binding and hydrolysis on dynamics of canine parvovirus NS1. J Virol. 84(10): 5391—5403.
- Moehler M. H., Zeidler M., Wilsberg V. et al. (2005). Parvovirus H-1-induced tumor cell death enhances human immune response in vitro via increased phagocytosis, maturation, and cross-presentation by dendritic cells. Hum Gene Ther. 16(8): 996—1005.
- Chow B. D., Esper F. P. (2009). The human bocaviruses: a review and discussion of their role in infection. Clin Lab Med. 29(4): 695—713.
2 Этиология и патогенез
Парвовирус B19V (ПВ) является вирусом, содержащим дезоксирибонуклеиновую кислоту (ДНК) в форме двадцатигранника, не имеющим оболочки. Геном представлен единственной цепочкой ДНК, кодирующей, помимо капсидных белков, один неструктурный белок, NS1.
Штамм B19V патогенен только для человека, а штаммы парвовируса животных не опасны для человека .
ПВ обладает высоким сродством к клеткам-предшественникам эритроцитов, которое обусловлено присутствием на их поверхности Р-антигена, благодаря которому вирус способен проникать внутрь клетки. Р-антиген обнаружен также на поверхности эритробластов, клеток эндотелия, трофобласта, печени плода и миокарда. Люди, у которых этот антиген отсутствует, не чувствительны к ПВ, а инфицирование не приводит к развитию аплазии эритроидного ростка .
После проникновения в клетку, ПВ запускает механизмы цитотоксического повреждения, приводящего к гибели клетки путем апоптоза. Лизис предшественников эритроцитов приводит к угнетению эритропоэза, уменьшению числа эритроцитов периферической крови, снижению концентрации гемоглобина и развитию анемии. Поражение плода развивается через 1-3 недели после заражения матери, для появления признаков водянки плода требуется еще примерно 4 недели .
Тяжелые проявления при внутриутробном инфицировании ПВ являются, в основном, результатом анемии, вызванной поражением эритроидного ростка кроветворения, но также могут быть вызваны гипоальбуминемией, миокардитом и плацентитом. В конечном итоге развивается сердечная недостаточность с последующей неиммунной водянкой и гибелью плода. Неиммунная водянка плода в 80% случаев развивается именно во втором триместре беременности (17-28 неделя гестации) .
Развитие сердечной недостаточности у плода может быть, как результатом тяжелой анемии, так и непосредственного воздействия ПВ на миокардоциты с последующим развитием миокардита . Плацентит, закономерно возникающий в ответ на внедрение ПВ, может привести к плацентарной недостаточности и неблагоприятным последствиям у плода, несмотря на отсутствие признаков его инфицирования.
Внедрение вируса вызывает активацию в основном гуморального звена иммунитета. Вирусемия, как правило, развивается приблизительно через 7 дней после инокуляции вируса и сохраняется на высоком уровне в большинстве случаев менее 7 дней. На 10-12 день после заражения (2-3 день после начала клинических проявлений острой инфекции), в сыворотке крови регистрируются специфические иммуноглобулины М (IgM), достигая максимального уровня к 21-24 дню. Персистенция IgM продолжается 2-3 месяца, в отдельных случаях до 6 месяцев.
Иммуноглобулины класса G (Ig G) определяются в крови на 24-28 день инфицирования (или спустя 7 дней после появления первых клинических проявлений). Ig G сохраняются в сыворотке крови в течение нескольких лет или пожизненно, реагируя повышением титра на повторное внедрение вируса. Описаны случаи персистенции вирусной ДНК в материнской крови в течение всей беременности, а также низкого уровня ДНК B19V в периферической крови и ткани костного мозга у иммунокомпетентных лиц в течение нескольких лет после первичной инфекции. Механизм этого явления неизвестен .
Имеются отдельные сообщения о связи этого заболевания плода с пороками центральной нервной системы (ЦНС), лицевой части черепа, глаз.
Диагностика
Диагноз CPV-2 подтверждают путем определения вируса или титров антител. Определение вируса через его выделение, электронную микроскопию, фекальную гемагглютинацию или иммуноферментный твердофазный анализ (ELISA) на присутствие антигенов к парвовирусной инфекции часто выполняется на фекалиях, ректальных мазках или биопсии кишечника пораженных животных. Наиболее практичным методом для большинства ветеринарных врачей является тест ELISA на парвовирусный антиген (CITE, Мехх). Анализ легко выполнить на фекалиях после ректального мазка. Несмотря на достаточную точность теста, животные с предположительным клиническими и лабораторными признаками, однако отрицательными результатами ELISA, должны рассматриваться как инфицированные парвовирусом до тех пор, пока не доказано обратное
Поскольку этот тест часто выполняется у недавно вакцинированных щенков, важно заметить, что производители вакцин признают возможность слабого положительного результата теста через 5-15 дней после вакцинации вследствие использования модифицированных живых парвовирусных вакцин
Возможные осложнения и сопутствующая симптоматика
Если у пострадавшего ребенка отсутствуют заболевания крови, временное снижение уровня гемоглобина и эритроцитов им переносится без особых сложностей Показатели приходят в норму спустя неделю или 10 суток. Однако при наличии гемолитической анемии либо иммунодефицита заболевание протекает достаточно тяжело:
- Если имеет место анемия, развитие инфекции запускает уничтожение популяции клеток костного мозга, формирование апластического криза. Начинаются проблемы с кроветворением, наблюдается нехватка фолиевой кислоты.
- В случае иммунодефицита развивается анемия хронического характера. Ее течение волнообразно, поскольку парвовирус постоянно циркулирует в системах организма. Детям и взрослым с таким осложнением потребуется постоянное переливание крови. Такое явление наблюдается в случае проведения химиотерапии, при наличии ВИЧ и врожденном иммунодефиците.
- Осложнения могут наблюдаться и у беременных женщин – если заражение имело место в процессе вынашивания ребенка, у плода высок риск развития водянки. Но подобное осложнение наблюдается в 10%, обычно парвовирус не воздействует на малыша негативно. Исключением является инфицирование в самом начале беременности, когда не исключается самопроизвольный аборт.
Перейдем к рассмотрению чаще всего встречающихся признаков патологии. У детей обычно наблюдается появление инфекционной эритемы, ее инкубационный период длится от 4 до 14 суток. Достаточно часто симптомы отсутствуют, в противном случае отмечают излишнюю бледность носогубного треугольника и ярко-красную пятнисто-папулезную сыпь, локализующуюся на щеках.
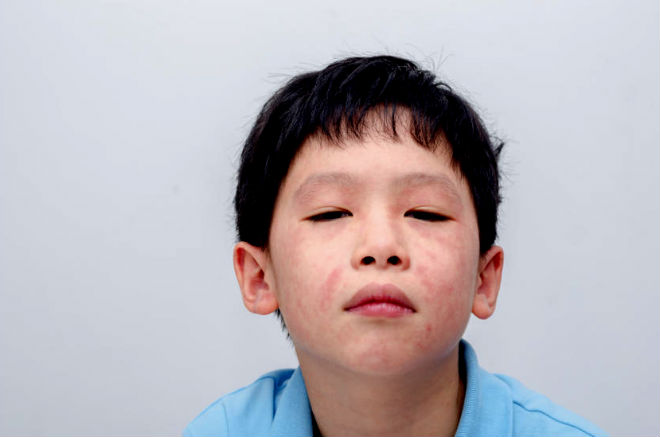 Такие высыпания подобны пятну от пощечины. Ребенок ощущает жжение на этих участках. На руках и ногах наблюдается кружевные либо сетчатые высыпания, часто сопровождающиеся субфебрильной температурой и состоящие из:
Такие высыпания подобны пятну от пощечины. Ребенок ощущает жжение на этих участках. На руках и ногах наблюдается кружевные либо сетчатые высыпания, часто сопровождающиеся субфебрильной температурой и состоящие из:
- папул;
- геморрагий;
- везикул.
Появление сыпи сопровождается сильным зудом, она проходит спустя пять или семь суток. Новые высыпания провоцируют эмоциональные встряски, воздействие прямых лучей солнца, излишняя физическая нагрузка, перепады атмосферного давления.
Парвовирусный артрит острого течения у детей формируется редко. Патология в большинстве случаев затрагивает периферические суставы и развивается у взрослых. Может наблюдаться болезненность в пораженной области, отеки тканей, покраснение кожного покрова, скованность в утренние часы. Чаще всего страдают кисти, суставы коленей. Длительность заболевания – три недели, после чего симптомы сходят на нет.
Заражение собак парвовирусной инфекцией
Парвовирус в больших концентрациях выделяется во внешнюю среду с фекалиями инфицированных животных через 4-5 дней после заражения, то есть до появления первых симптомов энтерита у собак. Выделения вируса продолжаются в течение всего периода болезни и примерно еще 10 дней после клинического выздоровления.
Парвовирусная инфекция проникает в организм здоровых собак через прямой контакт ротовой или носовой полости с зараженными фекалиями. Кроме того, возможно косвенное заражение контактированием через предметы обихода, одежду владельца и другие объекты, которые могли быть испачканы фекалиями больного животного.
Парвовирус у здоровых собак, первоначально развивается в лимфоидной ткани ротоглотки с последующим переходом в общесистемную форму в результате распространения по организму с кровотоком. Вирусная инфекция преимущественно заражает и разрушает быстро делящиеся клетки слизистого эпителия тонкой кишки, лимфопоэтические ткани (продуцирующие лимфоциты) и костный мозг. С этого момента начинают развиваться симптомы.
Уничтожение вирусом кишечных крипт приводит к эпителиальному некрозу слизистой оболочки (омертвлению), атрофии ворсинок, нарушению абсорбционной (всасывающей) способности кишечника. В результате эти патологические процессы приводят к разрушению функциональности кишечного защитного барьера, что заканчивается активным проникновением в кровь бактерий, находящихся в просвете кишечника и развитию вторичной инфекции.
Такая картина энтерита у щенков младше 8-недельного возраста, а также у старых собак может привести к развитию сердечных инфекций, воспалению сердечной мышцы и некрозу миокарда. Впоследствии миокардит может клинически проявляться как острая сердечно-легочная недостаточность с наличием или без симптомов парвовирусного энтерита. Стоит отметить, что у щенков сердечные проблемы наблюдаются не так часто, поскольку в их крови находятся антитела против парвовируса, полученные с молоком матери (колостральный иммунитет).
Treatment
At the moment, there are no treatments that directly target parvovirus B19 virus.Intravenous immunoglobulin therapy (IVIG) therapy has been a popular alternative because doctors can administer it without stopping chemotherapy drugs like MEL-ASCT. Also, the treatment’s side effects are rare as only 4 out of 133 patients had complications (2 had acute renal failure and 2 had pulmonary edema) even though 69 of the patients had organ transplants and 39 of them were HIV positive. This is a large improvement over administering rituximab.[citation needed] The monoclonal antibody against the CD20 protein has been shown to cause acute hepatitis, neutropenia via parvovirus B19 reactivations, and even persistent parvovirus B19 infection. However, it is important to note that IVIG therapy is not perfect as 34% of treated patients will have a relapse after 4 months.
Клиническое описание
Клинические симптомы различаются в зависимости от стадии и тяжести болезни (таблица 1). Тяжесть определяется дозой вирусного заражения, вирулентностью штамма и иммунной реакцией хозяина. Животные могут временно лихорадить и быть вялыми в начале виремии, при отсутствии желудочно-кишечных признаков. Анорексия, угнетение, рвота и диарея обычно наступают через 2-3 дня, при наличии или отсутствии лихорадки. Рвота часто бывает обильной и продолжительной, а диарея характеризуется водянистым объемным стула со слизью и свежей или переваренной кровью. Животные при попадании к ветеринарному врачу часто сильно дегидратированы.
| Таблица 1. Распространенные клинические симптомы и лабораторные аномалии, связанные с парвовирусной инфекцией собак | |
|---|---|
| Клинические симптомы | Лабораторные аномалии |
| Лихорадка | Лейкопения |
| Сонливость | Лимфопения |
| Анорексия | Нейтропения |
| Рвота | Анемия |
| Диарея с кровью | Гипопротеинемия |
| Дегидратация | Гипогликемия Гипокалиемия Гипонатриемия Гипохлоремия Метаболический ацидоз |
При парвовирусной инфекции обычно бывает лейкопения. Начальная лейкопения является результатом прямого вирусного лимфоцитолиза во время вирусемии. Хотя число лимфоцитов быстро уменьшается, почти в одно и то же время с началом желудочно-кишечных симптомов развивается значительная нейтропения. Нейтропении способствуют как периферическое нейтрофильное потребление (особенно в желудочно-кишечном тракте), так и разрушение клеток-предшественников в пределах костной ткани.
В число менее частых гематологических последствий парвовирусного энтерита входят анемия, тромбоцитопения и гипопротеинемия. Может произойти серьезная кровопотеря через желудочно-кишечный тракт, приводящая к анемии и гипопротеинемии. Поскольку у молодых щенков изначально меньше эритроцитов, они особенно подвержены анемии вследствие геморрагической диареи. Иногда происходит тромбоцитопения как следствие повышенного использования тромбоцитов в желудочно-кишечном тракте в сочетании с разрушением мегакариоцитарных предшественников в костном мозге.
В ходе биохимического анализа сыворотки крови обычно выявляют несколько аномалий. Гипогликемия и гипокалиемия могут быть результатами недостаточного поступления питательных веществ в организм молодых щенков. Рвота, диарея и дегидратация могут повлечь за собой метаболический ацидоз, гипонатриемию и гипохлоремию. Реже наблюдаются развитие предпочечной азотемии, повышение ферментов печени и гипербилирубинемия.
Осложнения парвовирусной инфекции, изменяющие клинические симптомы и лабораторные параметры, могут проявляться с самого начала или развиваются в ходе терапии. В число существенных осложнений входят септицемия или эндотоксемия, диссеминированная внутрисосудистая коагуляция (DIC), а также инвагинация кишечника. Сепсис и DIC происходят в результате нарушения функции кишечного барьера и нейтропении. Гипермоторика кишечника предрасполагает к инвагинации, клинические признаки которой (рвота и угнетение) могут быть легко приняты за ухудшение вирусной болезни. Осторожный и щадящий ежедневный осмотр является одним из важных моментов ухода за животными с парвовирусной инфекцией.
Диагностика
Парвовирусная инфекция опасна тем, что может протекать бессимптомно. Из-за инфекционной эритемы у детей заболевание часто определяют неверно, принимая его за схожую по внешним признакам корь, краснуху или скарлатину. Соответственно, пациента держат на карантине и считают, что он перенес определенное заболевание. Такая ошибка может иметь серьезные последствия.

Из-за схожести с другими заболеваниями и широким разбросом патологий, являющихся симптомами и осложнениями инфекции, необходимо проводить дифференциальную диагностику.
Обнаружить парвовирус можно следующими методами:
- Общий анализ крови. С помощью такой диагностики определяют морфологию эритроцитов, количество ретикулоцитов и тромбоцитов.
- Полимеразная цепная реакция. Это исследование позволяет выявить ДНК вируса.
- ИФА. Иммуноферментный анализ определяет в сыворотке крови специфические антитела (lgM и lgG).
- Радиоиммунный анализ. Проводится с той же целью, что ИФА. Оба метода относятся к серологическим исследованиям.
- Ультразвуковая диагностика. Имеет значение для беременных женщин. Позволяет выявить водянку плода.
- Анализ спинномозговой жидкости. Выявляет ДНК вируса.
Основное направление диагностики – дифференциация парвовируса от других заболеваний:
- кори;
- краснухи;
- скарлатины;
- железодефицитной анемии;
- энтеровирусной инфекции;
- псевдотуберкулеза;
- ВИЧ-инфекции;
- мононуклеозного синдрома.
Онколитическое действие парвовирусов
По всей вероятности, онкотропизм парвовирусов не связан с эффективным проникновением вируса в трансформированную клетку, а обусловлен преимущественной репликацией вируса в раковых клетках. При этом парвовирусы блокируют пути активации интерферонов первого типа, особенно в трансформированных фибробластах. Особую роль в онколитической активности парвовирусов играет основной неструктурный белок NS1.
Хеликазная активность NS1 необходима для репликации вируса, и он также является главным фактором, ответственным за онколитическую и цитотоксическую активность. Парвовирусный белок NS1 в относительно низкой концентрации способен вызвать гибель раковых клеток, но той же концентрации недостаточно для индукции апоптоза у клеток с нормальным фенотипом.
Парвовирусы могут также модулировать противоопухолевый иммунитет. В результате гибели опухолевых клеток, индуцированных парвовирусом, нередко высвобождаются антигены, характерные для раковых клеток и их молекулярные комплексы. Это стимулирует представление опухолевых антигенов иммунной системе организма и вызывает формирование более выраженного иммунного ответа против клеток опухоли.
Применение онколитических парвовирусов и векторных систем на их основе будет способствовать разработке подходов к лечению широкого круга болезней человека, в первую очередь онкологических заболеваний. Достигнутые в этой области успехи уже позволили перейти к проведению клинических испытаний для лечения злокачественных заболеваний.
Строение
Строение вирусной частицы. Вирионы диаметром 18—26 нм имеют икосаэдрический тип симметрии. Геном вируса содержит одноцепочечную ДНК
Вирионы парвовирусов представляют собой безоболочечные изометрические частицы с кубической симметрией диаметром 25 нм. Это довольно мелкие вирусы животных. Капсид парвовирусов состоит из 32 капсомеров диаметром 3—4 нм. Парвовирусы содержат одноцепочечную линейную ДНК размером 5,2 тн (19—32 % массы вирионов). Парвовирусы содержат 63—81 % белков. Сравнительным анализом некоторых автономных парвовирусов обнаружено различие в их структурных белках. Парвовирусы собак (ПВС), свиней (ПВСв), кошек (ПВК) и мышей (ПВМ) содержат по три структурных полипептида VP1, VP2, VP3 с молекулярной массой соответственно 79—82; 65—66 и 62—63 кД. Парвовирус крупного рогатого скота содержит четыре полипептида VP1, VP2, VP3 и VP4 с молекулярной массой соответственно 74,5; 67, 62 и 57 кД. Следует отметить, что у парвовируса свиней, выделенного при диарее (штамм Н-45), также обнаружено четыре структурных полипептида (81, 70, 66 и 62 кД). Основным белком у парвовирусов млекопитающих является VP3, на долю которого приходится около 80 % массы вирионных белков.
Капсид содержит 60 молекул белка VP2 (65 кД) и небольшое количество молекул VP1 (84 кД). VP1 и VP2 образуются альтернативным сплайсингом одной мРНК и полной последовательности VP2. Третий структурный белок VP3 образуется в полных (ДНК-содержащих) капсидах путём отщепления 15—20 аминокислот от аминоконца VP2. Зависимость размножения парвовируса от стадии клеточного цикла указывает на зависимость его репликации от репликации клеточной ДНК. Вирионы не содержат полимеразы, но способны кодировать такой фермент. Вместо этого используется клеточная полимераза И для транскрипции вирусной ДНК в двухспиральную промежуточную структуру, которая затем используется как матрица для других клеточных ферментов, катализирующих транскрипцию вирусных мРНК. Альтернативный сплайсинг структур приводит к увеличению отдельных видов мРНК, которые транслируются в большое количество различных белков. Наиболее обильный пул представлен мРНК, кодируемыми 3′-половиной генома, управляющей синтезом структурных белков. Неструктурный белок NS1, кодируемый 5′-половиной генома, также образуется в очень большом количестве и выполняет многие функции: 1) он связан с ДНК и требуется для репликации вирусной ДНК; 2) выполняет роль геликазы; 3) служит эндонуклеазой; 4) интерферирует с репликацией клеточной ДНК.
Эта активность ведет к остановке деления клеток в S фазе. Механизм репликации генома является удивительно комплексным. 3′-конец геномной (-)ДНК служит полупраймером для начала синтеза двуцепочечнои циркулярной ДНК в качестве репликативного предшественника. Одной из особенностей репликации геномной ДНК являлось образование димерной формы репликативного предшественника с последующим синтезом тетрамерной структуры, состоящей из двух полностью позитивных и двух полностью негативных цепей вирусной ДНК, которые с помощью эндонуклеазы превращаются в одноцепочечные молекулы, в том числе в потомство вирусной ДНК.